Новости
Нефтегазовая пром.
08.07.2025
Выставки
Наука и технология
20.06.2025
25.06.2025
Теги
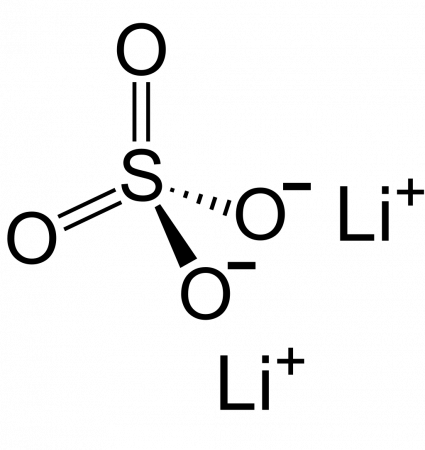
Сульфат лития
Сульфат лития
| Сульфат лития | |
|---|---|
 |
|
| Систематическое наименование |
Сульфат лития |
| Традиционные названия | Сернокислый литий |
| Хим. формула | Li2SO4 |
| Молярная масса | 109,94 г/моль |
| Плотность | 2,221 г/см³ |
| Температура | |
| • плавления | 859 °C |
| Мол. теплоёмк. | 117,57 Дж/(моль·К) |
| Энтальпия | |
| • образования | -1436,0 кДж/моль |
| Удельная теплота плавления | 9,3 кДж/моль |
| Растворимость | |
| • в воде | 34,320; 29,2100 г/100 мл |
| Рег. номер CAS | 10377-48-7 |
| PubChem | 66320 |
| Рег. номер EINECS | 233-820-4 |
| SMILES |
[Li+].[Li+].[O-]S(=O)(=O)[O-]
|
| InChI |
1S/2Li.H2O4S/c;;1-5(2,3)4/h;;(H2,1,2,3,4)/q2*+1;/p-2
INHCSSUBVCNVSK-UHFFFAOYSA-L
|
| RTECS | OJ6419000 |
| ChEBI | 53474 |
| ChemSpider | 59698 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Сульфат лития — соль щелочного металла лития и серной кислоты. Химическая формула Li2SO4. Образует кристаллогидрат Li2SO4•H2O.
Содержание
Получение
- Кристаллогидрат сульфата лития получают взаимодействием гидроксида или карбоната лития с серной кислотой с последующим упариванием:
-
- 2 LiOH + H2SO4 → Li2SO4 + 2 H2O
- Безводную соль получают нагреванием моногидрата выше 500°С.
Физические свойства
Безводный Сульфат лития образует три кристаллические модификации:
- α-форма — устойчивая при обычных условиях модификация с моноклинной решёткой, пространственная группа P 21/c, параметры a = 0,844 нм, b = 0,495 нм, c = 0,824 нм, β = 107,9°, Z = 4.
- β-форма — гексагональная решётка
- γ-форма — при температуре выше 575°С образует кубическую решётку, пространственная группа I 43m, a = 0,707 нм, Z = 4.
Кристаллогидрат образует кристаллы моноклинной сингонии, пространственная группа P 21, параметры a = 0,814 нм, b = 0,483 нм, c = 0,543 нм, β = 107,58°, Z = 4.
Химические свойства
- Взаимодействует с серной кислотой с образованием гидросульфата лития:
-
- Li2SO4 + H2SO4 → 2 LiHSO4
- Взаимодействием с соединениями бария удобно получать различные соединения лития:
-
- Li2SO4 + Ba(OH)2 → 2 LiOH + BaSO4↓
- Li2SO4 + Ba(N3)2 → 2 LiN3 + BaSO4↓
- При нагревании с водородом, аммиаком или углеродом (кокс) восстанавливается до сульфида лития:
-
- Li2SO4 + 4 C →800oC Li2S + 4 CO
Применение
Сульфат лития используется для изготовления головок детекторов в ультразвуковой дефектоскопии и как компонент люминофоров. Также он используется как средство для лечения маниакально-депрессивного психоза. Это вещество — пьезоэлектрик.
Физиологическое действие
Сульфат лития обладает средней токсичностью. Как и все соединения лития, влияет на ЦНС.
