Нитрид алюминия
Нитрид алюминия
| Нитрид алюминия | |
|---|---|
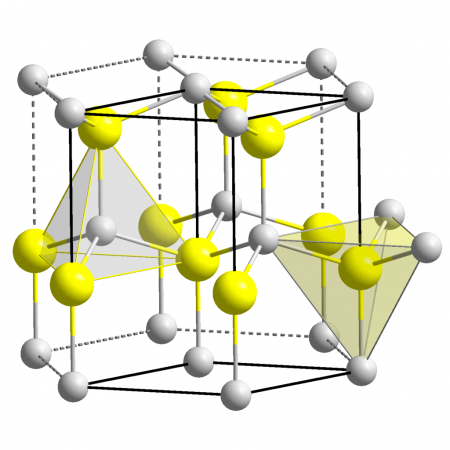 Al3+ N3− Al3+ N3− |
|
| Систематическое наименование |
Нитрид алюминия |
| Хим. формула | AlN |
| Состояние | порошок от белого до светло-жёлтого цвета |
| Молярная масса | 40,9882 г/моль |
| Плотность | 3,260 г/см³ |
| Температура | |
| • плавления | 2200 °C |
| • кипения | 2517 °C |
| Уд. теплоёмк. | 740 Дж/(кг·К) |
| Теплопроводность | 285 Вт/(м·K) |
| Растворимость | |
| • в воде | разлагается |
| Показатель преломления | 1,9–2,2 |
| Координационная геометрия | тетраэдральная |
| Кристаллическая структура | типа вюрцита |
| Рег. номер CAS | 24304-00-5 |
| PubChem | 90455 |
| Рег. номер EINECS | 246-140-8 |
| SMILES |
N#[Al]
|
| InChI |
1S/Al.N
PIGFYZPCRLYGLF-UHFFFAOYSA-N
|
| ChEBI | 50884 |
| ChemSpider | 81668 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Нитрид алюминия (алюмонитрид) — бинарное неорганическое химическое соединение алюминия с азотом. Химическая формула — AlN.
Содержание
История
Нитрид алюминия был впервые синтезирован в 1877 году, но только в середине 1980-х его потенциал для практического применения в микроэлектронике был осознан из-за его относительно высокой, для керамики, теплопроводности (70—210 Вт·м−1·K−1 для поликристаллического материала, и до 275 Вт·м−1·K−1 для монокристаллов). Этот материал представляет интерес как нетоксичная альтернатива оксиду бериллия. Методы металлизации позволяют применять данное вещество в электронике вместо глинозёма и оксида бериллия.
Физические свойства
Нитрид алюминия — (главным образом) материал с ковалентными связями, имеющий гексагональную кристаллическую структуру, известную как вюрцит. Кристаллографическая группа для этой структуры — C6v4 − P63mc.
Химические свойства
Белый порошок или водянисто-белые прозрачные кристаллы. Медленно растворяется в горячих минеральных кислотах. Холодные НCl, H2SО4, HNO3 и царская водка действуют слабо, холодная HF не действует. Концентрированные горячие растворы щелочей разлагают с выделением NH3. Материал устойчив к очень высоким температурам в инертных атмосферах. На воздухе поверхностное окисление происходит выше 700 °C, и при комнатной температуре были обнаружены поверхностные окисленные слои толщиной 5—10 нм. Этот окисный слой защищает материал до 1370 °C. Выше этой температуры происходит объёмное окисление материала. Нитрид алюминия устойчив в атмосферах водорода и углекислого газа до 980 °C. Материал медленно распадается в неорганических кислотах при контакте жидкости с границами зёрен, как и в случае с сильными щелочами. Материал медленно гидролизуется в воде.
Применение
- Производство светодиодов (полупроводник с шириной запрещённой зоны 6 эВ);
- Материалы из нановолокна;
- Материал для высокотеплопроводной керамики (вместо оксида бериллия) — подложки для производства высокочастотных резисторов, корпуса электронных схем.
Получение
Получается восстановлением Аl2O3 углем в атмосфере азота:
- Al2O3 + 3 C + N2 →1600−1800∘C 2 AlN + 3 CO ↑
Также Нитрид алюминия можно получить с помощью азотирования (без доступа кислорода) алюминиевой пудры:
- N2 + 2 Al →800−1200∘C 2 AlN
При пропускании через алюминий аммиака при нагревании:
- 2 Al + 2 NH3 →t>600∘C 2 AlN + 3 H2 ↑

