Новости
Нефтегазовая пром.
08.07.2025
Выставки
Наука и технология
20.06.2025
25.06.2025
Теги
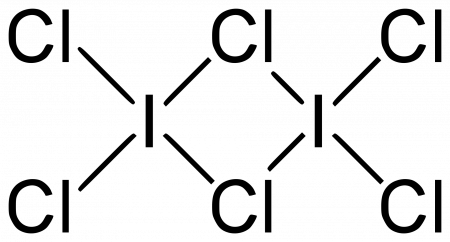
Гексахлорид дийода
Гексахлорид дийода
| Гексахлорид дийода | |
|---|---|
 |
|
| Систематическое наименование |
Гексахлорид дийода |
| Традиционные названия | Хлористый йод |
| Хим. формула | I2Cl6 |
| Состояние | оранжево-жёлтые кристаллы |
| Молярная масса | 466,53 г/моль |
| Плотность | 3,203 г/см³ |
| Температура | |
| • плавления | под давл. 101 °C |
| • кипения | разл. 64 °C |
| Рег. номер CAS | 865-44-1 |
| PubChem | 70076 |
| Рег. номер EINECS | 212-739-8 |
| SMILES |
ClI(Cl)Cl
|
| InChI |
1S/Cl3I/c1-4(2)3
PAWIVBWALDNUJP-UHFFFAOYSA-N
|
| ChemSpider | 63265 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Гексахлорид дийода — бинарное неорганическое соединение йода и хлора с формулой I2Cl6, оранжево-жёлтые кристаллы, реагирует с водой.
Содержание
Получение
- Растворение иода в избытке жидкого хлора:
-
- I2 + 3 Cl2 →−78oC I2Cl6
- В расплаве монохлорида иода происходит обратимая реакция:
-
- 6 ICl ⇄ I2Cl6 + 2 I2
Физические свойства
Гексахлорид дийода образует оранжево-жёлтые кристаллы.
Расплав является электролитом, содержит ионы ICl2+ и ICl4—.
Химические свойства
- Разлагается при незначительном нагревании:
-
- I2Cl6 →64−77oC 2 ICl + 2 Cl2
- Реагирует с холодной водой:
- и с горячей:
- С концентрированной соляной кислотой или хлоридами щелочных металлов образует комплексы:
- Реагирует с щелочами:
- Является сильным окислителем:
