Новости
Нефтегазовая пром.
08.07.2025
Выставки
Наука и технология
20.06.2025
25.06.2025
Теги
Перхлорат серебра
Перхлорат серебра
| Перхлорат серебра | |
|---|---|
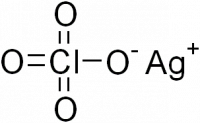 |
|
| Систематическое наименование |
Перхлорат серебра |
| Традиционные названия | Хлорнокислое серебро |
| Хим. формула | AgClO4 |
| Состояние | бесцветные кристаллы |
| Молярная масса | 207,32 г/моль |
| Плотность | 2,806 г/см³ |
| Температура | |
| • разложения | 486 °C |
| Растворимость | |
| • в воде | 54525; 792,899 г/100 мл |
| Рег. номер CAS | 7783-93-9 |
| PubChem | 24562 |
| Рег. номер EINECS | 232-035-4 |
| SMILES |
[Ag+].[O-]Cl(=O)(=O)=O
|
| InChI |
1S/Ag.ClHO4/c;2-1(3,4)5/h;(H,2,3,4,5)/q+1;/p-1
YDHABVNRCBNRNZ-UHFFFAOYSA-M
|
| ChemSpider | 22968 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Перхлорат серебра — неорганическое соединение, соль металла серебра и хлорной кислоты с формулой AgClO4, бесцветные кристаллы, растворяется в воде, образует кристаллогидрат.
Содержание
Получение
- Действие избытка хлорной кислоты на Нитрат серебра I при нагревании:
-
- 4 AgNO3 + 4 HClO4 →T 4 AgClO4 + 4 NO2 ↑ + O2 ↑ + 2 H2O
- Действие перхлората бария на Сульфат серебра:
-
- Ag2SO4 + Ba(ClO4)2 → 2 AgClO4 + BaSO4 ↓
- Растворением серебра в концентрированной хлорной кислоте:
2 Ag + 3 HClO4 → 2 AgClO4 + HClO3 + H2O
- Растворением оксида серебра I в хлорной кислоте.
Физические свойства
Перхлорат серебра образует быстро расплывающиеся на воздухе бесцветные кристаллы, кубической сингонии, пространственная группа F 43m, параметры ячейки a = 0,701 нм, Z = 4.
Хорошо растворяется в воде, этаноле, диэтиловом эфире, толуоле.
Образует кристаллогидрат состава AgClO4•H2O. Из аммиачных растворов выделяются аддукты вида [Ag(NH3)2]ClO4•H2O
Применение
- Катализатор в органической химии.